Ингаляционная терапия риносинусита
Статья о применении ингаляционного прибора PARI SINUS в лечении бактериального риносинусита:
"Ингаляционная терапия нетяжелых форм острого бактериального риносинусита"
Научно-практический журнал для врачей "Медицинский совет" №6 2018г
Авторы: И.Б.Анготоева (1), Д.С.Пшенников (2)
(1) Российская медицинская академия непрерывного профессионального образования Минздрава России, Москва
к.м.н. Россия
(2) Рязанский государственный медицинский университет им. акад. И.П. Павлова Минздрава России, Клиническая больница им. Н.А. Семашко Россия
ИНГАЛЯЦИОННАЯ ТЕРАПИЯ
НЕТЯЖЕЛЫХ ФОРМ ОСТРОГО БАКТЕРИАЛЬНОГО РИНОСИНУСИТА
Эпидемиологические исследования во всем мире показывают, что воспалительные заболевания носа и околоносовых пазух (ОНП) являются ведущими в оториноларингологии по частоте обращаемости как в поликлиники, так и в стационары. Несмотря на то что подавляющее большинство случаев острого риносинусита обусловлены вирусной инфекцией, антибактериальные препараты назначаются более чем в 80% случаев, что усугубляет проблему антибактериальной резистентности в современном мире. Решить эту проблему может локальная доставка препарата в полость носа и ОНП при помощи ингаляционного комплекса «Пари Синус» (компрессор и небулайзер).
Цель. Сравнить результаты топического ингаляционного лечения острого бактериального риносинусита (ОБРС) и стандартной системной антибиотикотерапии.
Материалы и методы. В открытое рандомизированное контролируемое исследование вошло 60 пациентов с ОБРС средней степени тяжести в возрасте от 19 до 62 лет. В основную группу вошли 30 человек, которым в течение 7 дней проводилась ингаляционная терапия на аппарате «Пари Синус» комбинированным препаратом Флуимуцил-антибиотик ИТ (тиамфеникола глицинат ацетилцистеинат, фармацевтическая компания «Замбон», Италия) в дозе 500 мг 1 раз в сутки. Контрольная группа (30 пациентов) 7 дней получала стандартную системную антибиотикотерапию амоксициллином 875
мг и клавулановой кислотой 125 мг 2 раза в сутки (Аугментин 2, «ГлаксоСмитКляйн», Великобритания). В результате оценивали динамику симптомов ОБРС, риноэндоскопическую картину и данные передней активной риноманометрии (ПАРМ). Результаты. В обеих исследуемых группах отмечено статистически значимое улучшение клинической симптоматики после лечения, что подтверждается данными риноэндоскопии и ПАРМ.
Вывод. Топическая ингаляционная терапия может оказаться более предпочтительной в отношении нетяжелых форм ОБРС по сравнению с системной антибиотикотерапией. При сходной эффективности потенциальная вероятность нежелательных реакций и развития антибиотикорезистентности значительно выше в группе системной антимикробной терапии.
Ключевые слова: острый риносинусит, топическая ингаляционная терапия, N-ацетилцистеин, тиамфеникол, «Пари Синус».
О причине широкого распространения терапия острого риносинусита (ОРС) является крайне актуальной проблемой в современной оториноларингологии. Согласно Европейским рекомендациям по лечению риносинусита (EPOS-2012), заболеваемость ОРС за последние 20 лет возросла почти в 2 раза и составляет от 6 до 15% популяции [1]. Известно, что воспалительные заболевания носа и околоносовых пазух (ОНП) являются ведущими по частоте обращаемости как в поликлиники, так и в стационары [2]. Эти данные обусловлены высоким уровнем острых респираторных вирусных инфекций (ОРВИ), которые чаще других становятся причиной ОРС [3].
Согласно EPOS-2012, по этиопатогенезу и, соответственно, тяжести клинических проявлений выделяют острые респираторные вирусные инфекции, острый поствирусный риносинусит и острый бактериальный
риносинусит (ОБРС) [1]. Известно, что практически каждый человек переносит от 2 до 5 эпизодов ОРВИ в год, из которых только 0,5–2% осложняются ОБРС [4]. Несмотря на высокую частоту вирусной инфекции при ОРС, системные антибактериальные препараты назначаются более чем в 80% случаев [5]. Однако многочисленные наблюдения свидетельствуют о том, что антибактериальная терапия при этом не влияет на течение заболевания и не уменьшает вероятность осложнений, но увеличивает частоту побочных реакций и рост бактериальной резистентности [6].
Совершенствование лечебной тактики пациентов с ОБРС является актуальной и нерешенной задачей в связи с широкой распространенностью риносинусита, сложностью получения материала для быстрого установления этиологического фактора при необходимости пункции ОНП, растущей резистентностью микроорганизмов. Задача усложняется отсутствием достоверных методов
дифференциальной диагностики вирусной и бактериальной этиологии заболевания. Из-за низкого уровня чувствительности и специфичности ни один из дополнительных визуализирующих методов диагностики (рентгенография, ультразвуковая диагностика, компьютерная томография) не может использоваться рутинно для постановки диагноза неосложненного ОБРС [5]. Таким образом, основным методом дифференциальной диагностики вирусного и бактериального ОРС по-прежнему остается анализ клинических данных, что влечет за собой высокую частоту ошибок при постановке диагноза, которая, по
разным данным, составляет около 50% [4].
Ведущее место в лечении ОБРС занимает системная антибиотикотерапия, которая показана при тяжелом и средней тяжести инфекционном процессе [3]. В большинстве случаев системная антибиотикотерапия назначается эмпирически на основании предполагаемой структуры возбудителей. Важное значение при этом отводится критериям отбора пациентов с выраженной клинической симптоматикой (табл. 1).

Однако ОРС даже бактериальной природы в большинстве случаев самостоятельно купируется без всякого лечения, тем более антибактериального. По данным плацебоконтролируемых исследований, частота спонтанного выздоровления высока и колеблется в пределах 50–70% [7]. Существуют исследования, показывающие отсутствие преимуществ лечения неосложненного ОБРС антибиотиками по сравнению с плацебо [8]. Это обстоятельство очень важно с учетом того, что проблема антибактериальной резистентности остро стоит в современном мире.
В случаях нетяжелого неосложненного течения ОБРС с целью уменьшения вреда системной антибиотикотерапии оправданно топическое применение препаратов. Все местные медикаменты в виде спрея или капель для лечения ОРС действуют ограниченно только в полости носа, в основном в зоне общего носового хода [9]. Решить эту проблему может ингаляционный способ доставки лекарственного препарата. В настоящее время широкое распространение получили небулайзерные ингаляции (аэрозольтерапия), которые образуют не менее 50% лекарственных частиц размером от 1 до 5 мкм [10]. Этот вид лечения заболеваний дыхательных путей существует длительное время, теоретически обоснован и клинически эффективен, но чаще ассоциируется с лечением патологии нижних дыхательных путей. Основной целью ингаляционной терапии является достижение максимального терапевтического эффекта при топическом применении в дыхательных путях и значительном снижении системных нежелательных реакций [11]. По нашему мнению, по аналогии со всей дыхательной системой ингаляционная терапия при ОРС является наиболее предпочтительной, так как лекарственный препарат действует непосредственно в месте патологического процесса при большей площади контакта.
Для терапии заболеваний полости носа и ОНП в России зарегистрирован ингаляционный комплекс «Пари Синус» (компрессор и небулайзер, Германия). «Пари Синус» является эффективным терапевтическим устройством с использованием лекарственных средств в аэрозольной форме. Прибор осуществляет подачу аэрозоля в режиме пульсации, что позволяет достигать осаждения препарата непосредственно в ОНП и оставаться там более продолжительное время, что создает ряд неоспоримых преимуществ (табл. 2) [11–13].

Препаратом выбора для ингаляционной терапии ОБРС является тиамфеникола глицинат ацетилцистеинат (ТГА) (Флуимуцил-антибиотик ИТ, фармацевтическая компания
«Замбон», Италия), представляющий собой комбинацию антибиотика тиамфеникола глицината и муколитика N-ацетилцистеина. Препарат входит в Российские стандарты и клинические рекомендации лечения ОРС и разрешен для введения в ОНП и ингаляционной терапии [3, 14].
Тиамфеникол является синтетическим производным природного антибиотика хлорамфеникола (левомицетина). В молекуле Тиамфеникола отсутствует нитрогруппа (NO2), с которой связывают образование токсичных нитропроизводных и развитие побочных эффектов при использовании хлорамфеникола, таких как миелотоксичность, рвота, гиперрастяжимость брюшной стенки, кардиоциркуляторный коллапс [15]. Тиамфеникол достаточно активен в отношении не только наиболее частых возбудителей респираторных инфекций (Streptococcus pneumoniaeHaemophilus influenzaе, Moraxella catarrhalis, Streptococcus
pyogenes, Staphylococcus aureus), а также в отношении многих штаммов, устойчивых к бета-лактамным антибиотикам,
внутриклеточным возбудителям (Legionella, Сhlamidia, Mycoplasma). Таким образом, Тиамфеникол обладает схожей активностью по сравнению с хлорамфениколом при значительно лучшем профиле безопасности [16]. N-ацетилцистеин оказывает прямое муколитическое действие, разрушая дисульфидные связи между молекулами мукополисахаридов секрета, и мукорегуляторное, увеличивая секрецию бокаловидными клетками менее вязких муцинов. Таким образом, за счет снижения вязкости мокроты и усиления двигательной активности ресничек мерцательного эпителия улучшается мукоцилиарный транспорт, что позволяет антибиотику тиамфениколу преодолевать сопротивление, связанное с вязкостью секрета [17]. Необходимо отметить, что N-ацетилцистеин обладает рядом свойств, имеющих значение при бактериальных инфекциях (табл. 3)

Таким образом, высокая активность и хорошая переносимость при отсутствии значимых побочных эффектов позволяют рекомендовать назначение препарата Флуимуцил®-антибиотик ИТ в качестве стартовой терапии нетяжелых форм ОРС.
С учетом вышеизложенного было проведено открытое рандомизированное сравнительное исследование в параллельных группах.
Цель. Сравнить результаты лечения пациентов с ОБРС средней степени тяжести при помощи ингаляционного комплекса «Пари Синус» комбинированным препаратом ТГА по сравнению со стандартной системной антибиотикотерапией амоксициллином 875 мг и клавулановой кислотой 125 мг (Аугментин 2, «ГлаксоСмитКляйн», Великобритания).
МАТЕРИАЛЫ И МЕТОДЫ
В исследование было включено 60 пациентов с диагнозом ОБРС средней степени тяжести, подтвержденным на основании данных анамнеза, клинического осмотра, включающего риноэндоскопическое исследование. Согласно EPOS-2012 [1], определение степени тяжести ОРС базируется на субъективной оценке своего состояния пациентом по 10-сантиметровой визуально-аналоговой шкале (ВАШ) (4–7 баллов на шкале соответствуют среднетяжелой форме заболевания). Обследуемые случайным образом были разделены на 2 группы по 30 человек. Рандомизация проводилась в соответствии с
компьютерным генератором случайных цифр. В основную группу (№1) вошли 30 человек с диагнозом ОБРС средней степени тяжести – 13 мужчин и 17 женщин от 19 до 59 лет. Этим пациентам в качествелечения проводилась пульсирующая ингаляционная терапия на аппарате «Пари Синус» комбинированным препаратом ТГА. Длительность ингаляции составила 6 мин (по 3 мин на каждую половину носа). Для приготовления ингалируемого раствора 500 мг препарата растворяли в 4 мл воды для инъекций. Курс терапии – 7 дней по одной ингаляции в день. При необходимости перед процедурой пациентам проводился немедикаментозный туалет полости носа при помощи аспирации патологического секрета. В контрольную группу (№2) вошли 30 человек с диагнозом ОБРС средней степени тяжести – 14 мужчин и 16
женщин от 20 до 62 лет. Этим пациентам в качестве лечения проводилась монотерапия стандартным антибиотиком амоксициллином клавуланатом (875 мг амоксициллина + 125 мг клавулановой кислоты). Курс терапии – 7 дней внутрь по 1 таблетке 2 раза в день. Всем испытуемым дважды (период Т0 до лечения и период Т1 через 7 дней после лечения) проводились следующие исследования:
- Субъективная оценка пациентом основных симптомов ОБРС по 5-балльной ВАШ E. Hultcrantz. Оценивалась сумма баллов следующих симптомов:
■ затруднение носового дыхания (заложенность носа, назальная обструкция);
■ выделения из носа (в т. ч. выделения, стекающие по задней стенке глотки);
■ боль или чувство давления (распирания) в проекции околоносовых пазух;
■ гипосмия.
- Субъективная оценка врачом состояния слизистой оболочки полости носа с помощью риноэндоскопического исследования. По 3-балльной ВАШ оценивались следующие признаки воспаления слизистой оболочки полости носа:
■ гиперемия;
■ отек;
■ наличие патологического секрета.
3. Передняя активная риноманометрия (ПАРМ) – метод для определения функции носового дыхания. Исследование проводилось при помощи риноманометра ATMOS РС 300 (Германия). Основные количественные показатели ПАРМ – суммарный объемный поток (СОП) и суммарное сопротивление (СС) воздушному потоку в точке фиксированного давления 150 Пa. Статистическая обработка полученных данных проводилась с помощью программы Microsoft Excel 2013 и пакета статистических программ STATISTICA 8.0. Для сравнения количественных различий признаков, подчиняющихся нормальному распределению, использовали t-критерий Стьюдента. Значимость различий в случае количественных признаков, не подчиняющихся нормальному распределению, оценивалась по критерию Вилкоксона. Различия считались достоверными в случае р<0,05.
Для определения результатов лечения в обеих группах использовали среднюю оценку суммы вышеперечисленных симптомов ОБРС (затруднение носового дыхания,выделения из носа, боль или чувство давления (распирания) в проекции околоносовых пазух, гипосмия) (рис. 1).
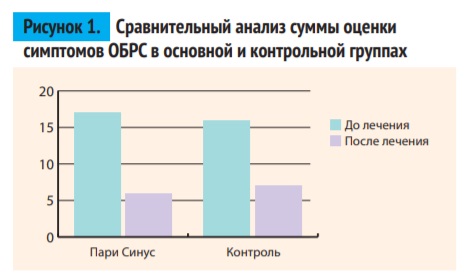
Средняя оценка суммы симптомов до лечения в основной и контрольной группе составила 17,2 ± 1,1 и 16,7 ± 1,0 балла соответственно, после лечения – 6,5 ± 0,2 и 6,9 ± 0,3. В обеих группах отмечено статистически значимое (p<0,05) улучшение клинической симптоматики после лечения. Разницей в оценке симптомов в пределах 0,5 балла можно пренебречь как клинически незначимой. Для определения результатов эндоскопического исследования также оценивали среднюю оценку суммы вышеперечисленных признаков воспаления слизистой оболочки носа (гиперемия, отек, наличие патологического секрета) (рис. 2). Средняя оценка суммы симптомов воспаления слизистой оболочки до лечения в основной и контрольной группах составила 8,2 ± 0,5 и 8,1 ± 0,5 балла соответственно, после лечения – 2,9 ± 0,2 и 3,1 ± 0,3. В обеих группах отмечено статистически значимое (p<0,05) улучшение эндоскопической картины после лечения. Разницей в оценке симптомов в пределах 0,2 балла можно пренебречь как клинически незначимой. Результаты ПАРМ (СОП и СС) представлены в таблице 4. В обеих группах отмечено сходное и статистически значимое (p<0,05) увеличение СОП и уменьшение СС, что говорит о достоверном улучшении клинической симптоматики после лечения.


ВЫВОДЫ
1. Обе исследуемые терапевтические тактики оказались эффективными в отношении ОБРС средней степени тяжести, что подтверждается улучшением клинической симптоматики, данными передней активной риноманометрии и риноэндоскопического исследования.
2. Топическая ингаляционная терапия на аппарате «Пари Синус» при использовании комбинированного лекарственного препарата тиамфеникола глицината ацетилцистеината (Флуимуцил-антибиотик ИТ) может оказаться более предпочтительной в отношении нетяжелых форм ОБРС по сравнению с системной антибиотикотерапией. При сходной эффективности потенциальная вероятность нежелательных реакций и развития антибиотикорезистентности значительно выше в группе системной антимикробной терапии.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов в ходе написания данной статьи.
ЛИТЕРАТУРА
1. Fokkens WJ, Lund VJ, Mullol J Bachert C, Alobid I, Baroody F et al. EPOS 2012: European position paper on rhinosinusiyis and nasal polyps 2012. A summary for otorhinolaryngologists. Rhinology, 2012, 50(1): 1–12. doi: 10.4193/Rhino50E2.
2. Минздравсоцразвития России. Заболевае мость населения России в 2007 г. Статисти ческие данные. Часть I. 2008. / Minzdravsots razvitiya Rossii. Zabolevaemost’ naseleniya Rossii v 2007 g. Statisticheskie dannye. Chast’ I. 2008.
3. Абдулкеримов Х.Т., Гаращенко Т.И., Кошель В.И., Рязанцев С.В., Свистушкин В.М. Принципы этиопатогенетической терапии острых синуситов: методические рекомендации. Под ред. С.В. Рязан цева. СПб.: Полифорум Групп, 2014./ Abdulkerimov Kh.T., Garashchenko T.I., Koshel’ V.I., Ryazantsev S.V., Svistushkin V.M. Printsipy etiopatogeneticheskoi terapii ostrykh sinusitov: metodicheskie rekomendatsii. Pod red. S.V. Ryazan tseva. SPb.: Poliforum Grupp, 2014. (In Russ.).
4. Свистушкин В.М., Савватеева Д.М. Современные тенденции в лечении пациентов с острым риносинуситом. РМЖ. Оториноларингология, 2016, 4: 251–254. / Savvateeva D.M., Svistushkin V.M. Current trends in the treatment of acute rhinosinusitis. RMJ. Оtorhinolaryngology, 2016, 4: 251–254.
5. Anon JB, Jacobs MR, Poole MD, Ambrose PG, Benninger MS, Hadley JA, Craig WA. Antimicrobial treatment guidelines for acute bacterial rhinosinusitis. Otolaryngol Head Neck Surg, 2004 Jun, 130(6): 794-6. doi: 10.1016/j.otohns.2003.12.003
6. Gill JM, Fleischut P, Haas S, Pellini B, Crawford A, Nash DB. Use of antibiotics for adult upper respiratory infections in outpatient settings: a national ambulatory network study. Family medicin, 2006, 38: 349-354.
7. Носуля Е.В. Антибиотики в комплексной терапии бактериального риносинусита: возможности и ограничения. Российская ринология, 2014, 22(3): 36-40. / Nosulia E.V. Antibiotics in the combination therapy of bacterial rhinosinusitis: Possibilities and limitations. Rossiiskaya rinologiya. 2014, 22(3): 36-40.
8. Hochhaus G. Pharmacokinetic/pharmacodynamic profile of mometasone furoate nasal spray: potential effects on clinical safety and efficacy. Clin Ther, 2008, 30: 1-13.
9. Möller W, Schuschnig U, Meyer G, Mentzel H, Keller M. Ventilation and drug delivery to the paranasal sinuses: studies in a nasal cast using pulsating airflow. Rhinology, 2008, 46(3): 213–220.
10. Boe J, Dennis JH. European Respiratory Society Nebulizer Guidelines: echnical Aspects. Eur Respir Rev. 2000, 72(10): 1-237.
11. Пшенников Д.С. Анготоева И.Б. Перспективы ингаляционной терапии острого риносинусита. Наука молодых, 2017, 2: 277-282. doi:
10.23888/HMJ20172277-282. / Pshennikov D.S., Angotoeva I.B. The prospects for inhalation therapy of rhinosinusitis. Eruditio Juvenium. 2017, 2: 277-282. doi: 10.23888/HMJ20172277-282.
12. Dennis JH. A review of issues relating to nebulizer standards. J Aerosol Med, 1998, 11 Suppl 1: S73–79.
13. Möller W, Schuschnig U, Celik G, Münzing W, Bartenstein P et al. Topical drug delivery in chronic rhinosinusitis patients before and after sinus surgery using pulsating aerosols. PLoS ONE, 2013, 8(9): e74991. doi:
10.1371/journal.pone.0074991. http: //journals.plos.org/plosone/article?id=10.1371/journal.pone.0074991. Ссылка активна на 4.12.16.
14. Колосова Н.Г., Дронов И.А. Топическая ингаляционная антибактериальная терапия респираторных инфекций у детей. РМЖ, 2017, 5: 319-321. / Kolosova N.G., Dronov I.A. Topical inhalation antibacterial therapy of respiratory infections in children. RMJ, 2017, 5: 319–321.
15. Mazzei T. Thiamphenicol: pharmacokinetic and safety considerations. GIMMOC, 2000, 4: 15–19.
16. Рациональная антимикробная фармакотерапия. Руководство для практикующих врачей. Под ред. Яковлева В.П., Яковлева С.В. М.: Литтерра, 2003. 1008 с. / Racional’naja antimikrobnaja farmakoterapija. Rukovodstvo dlja praktikujushhih vrachej. Pod red. Jakovleva V.P., Jakovleva S.V. M.: Litterra, 2003. 1008 s.
17. Чучалин А.Г., Соодаева С.К., Авдеев С.Н. Флуиму цил: механизмы действия и значение в терапии заболеваний органов дыхания. М.: Zambon Group S.P.A, 2004. / Chuchalin A.G., Soodaeva S.K., Avdeev S.N. Fluimucil: mehanizmy dejstvija i znachenie v terapii zabolevanij organov dyhanija. M.: Zambon Group S.P.A, 2004 (in Russian)
18. Dinicola S., De Grazia S., Carlomagno G., Pintucci J.P. N-acetylcysteine as powerful molecule to destroy bacterial biofilms. A systematic review. Eur Rev Med Pharmacol Sci. 2014, 18(19): 2942–2948.
19. Aslam S, Darouiche RO. Role of antibiofilm-antimicrobial agents in controlling device-related infections. Int J Artif Organs, 2011, 34 (9):
752–758.
